haloo several cutters :)
Okee sebelumnya saya akan menjelaskan terlebih dahulu apa itu Google form, Google form merupakan salah satu aplikasi online milik Google. Kita dapat membuat kuesioner, form, survery, dan quiz menggunakan app ini. Responden dapat menjawab form tersebut hampir di semua web browser termasuk di browser smartphone dan tablet. Jawaban dari resonden akan terlampir secara otomatis di sebuah halaman (seperti di excel), dan yang paling penting, applikasi online besutan Google ini dapat kita gunakan secara gratis !! :D
sebagai contoh silahkan lihat salah satu form saya berikut (Form hanya sebagai contoh, tengtang travel Booking) :
klik disini
------------------------------------------------------------------------------------------------------------
Baiklah, sebelum kita bahas bagaimana cara membuat form tersebut, pastikan terlebih dahulu kalian sudah memiliki akun gmail.
Langkah pertama, Log in ke gmail kalian, kemudian klik logo 'Google Apps' dan klik lagi 'Google drive'
(klik gambar 1 untuk lebih jelasnya)
Saya akan memberikan informasi tentang bagaimana membuat form, kuesioner, atau sejenisnya dengan memanfaatkan salah satu aplikasi dari Google apps, yaitu 'Google Form'
Okee sebelumnya saya akan menjelaskan terlebih dahulu apa itu Google form, Google form merupakan salah satu aplikasi online milik Google. Kita dapat membuat kuesioner, form, survery, dan quiz menggunakan app ini. Responden dapat menjawab form tersebut hampir di semua web browser termasuk di browser smartphone dan tablet. Jawaban dari resonden akan terlampir secara otomatis di sebuah halaman (seperti di excel), dan yang paling penting, applikasi online besutan Google ini dapat kita gunakan secara gratis !! :D
sebagai contoh silahkan lihat salah satu form saya berikut (Form hanya sebagai contoh, tengtang travel Booking) :
klik disini
------------------------------------------------------------------------------------------------------------
Baiklah, sebelum kita bahas bagaimana cara membuat form tersebut, pastikan terlebih dahulu kalian sudah memiliki akun gmail.
Langkah pertama, Log in ke gmail kalian, kemudian klik logo 'Google Apps' dan klik lagi 'Google drive'
(klik gambar 1 untuk lebih jelasnya)
Gambar 1
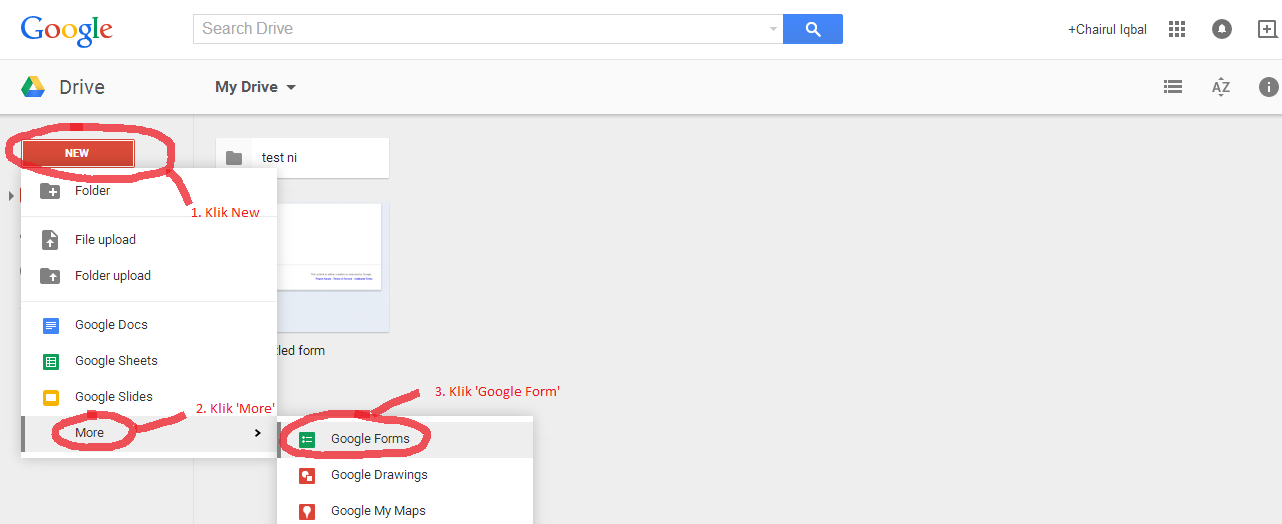
Langkah berikutnya, Klik 'New' di sebelah kiri, kemudian 'More' dan pilih 'Google Form' (Lihat gambar 2)
Gambar 2
Dan kalian sudah berhasil membuat online form :D
Sekarang kita bahas cara pengoprasiannya ( lihat gambar 3 untuk pedoman, penjelasan di bawah gambar)
Gambar 3
1. Klik 'Untitled Form' untuk menulis judul Form kalian
2. Klik 'Change Theme' untuk mengganti tema form (tema tidak akan terlihat di mode edit)
3. Klik 'View Responses' untuk melihat jawaban responden di spreadsheet
3. Klik 'View Live Form' untuk melihat pratinjau form (akan terbuka di tab baru), copy link di tab tersebut dan berikan kepada responden kalian
4. Pastikan semua hasil kerja kalian tersimpan secara otomatis.
itu saja penjelasan singkatnya, untuk model-model pertanyaan kuesioner dan fitur-fitur lainnya silahkan cutters explore sendiri :D
Sampai jumpa di postingan berikutnya :)

.png)
.png)
.png)











































